19 KiB
| title | author | date | lang | resumen | keywords | figureTitle | figPrefix | tableTitle | tblPrefix | eqnPrefix | secPrefix | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Análisis de la variación de la resistencia eléctrica en una celda de electrólisis alcalina mediante curvas de polarización I-V |
|
January 2026 | es | El presente estudio realiza un análisis preliminar del comportamiento de la resistencia eléctrica de una celda de electrólisis alcalina mediante las curvas de polarización I-V. La planta experimental está conformada por una celda con electrodos planos de acero inoxidable-304 y una solución de $NaOH$ 1 M. El sistema es alimentado mediante una fuente programable en corriente directa y monitoreado con instrumentos de alta precisión. Para la adquisición y control de variables se desarrolló una interfaz gráfica basada en Python 3 con comunicación mediante PyVISA, incorporando además un sensor PT1000 para el seguimiento de la temperatura del medio. La metodología experimental se compone de cuatro rondas consecutivas de curvas de polarización, realizadas con el mismo par de electrodos y el mismo electrolito, a fin de evaluar posibles variaciones en la respuesta de la resistencia eléctrica. Una vez finalizada la caracterización, se estima el valor de dicha resistencia, se grafican los datos obtenidos sobre la curva de polarización y se delimitan las posibles zonas de operación. Bajo este enfoque, se propone que la resistencia eléctrica puede utilizarse como una variable de apoyo para analizar el comportamiento del electrolizador e identificar regiones asociadas con pérdidas electroquímicas. |
|
Figura |
|
Tabla |
|
|
|
Introducción
Los sistemas de electrólisis alcalina del agua han optimizado su rendimiento gracias al avance en la innovación de nuevos materiales y estrategias de integración para electrodos, membranas y electrólito [@ref39]. Estos componentes constituyen una parte esencial de los electrolizadores, los cuales pueden estar formados por una o más celdas electroquímicas conectadas en serie o en paralelo [@ref43]. En este contexto, la evaluación del desempeño electroquímico suele realizarse mediante curvas de polarización, ya que estas permiten caracterizar la respuesta del sistema en diferentes regiones de operación [@ref39;@ref59].
En particular, las curvas Corriente-Voltaje (I-V), también conocidas como curvas de polarización, permiten evaluar cuantitativamente el comportamiento de la celda y distinguir las principales contribuciones a las pérdidas del sistema. Entre ellas se encuentran la polarización por activación, asociada con la cinética de la reacción electroquímica; la polarización óhmica, relacionada con la conducción eléctrica e iónica; y las limitaciones por transferencia de masa, también denominadas polarización de concentración [@ref11;@ref60].
Entre las contribuciones asociadas a las pérdidas del sistema, la resistencia óhmica desempeña un papel determinante, ya que su reducción permite operar a mayores densidades de corriente y mejorar el desempeño global del electrolizador [@ref59;@ref60]. En este sentido, diversos estudios han señalado que dicha resistencia puede incrementarse por múltiples factores, tales como la formación de nanoburbujas en las interfaces electrodo-electrolito, la selección de materiales y acabados superficiales que modifican la resistencia de contacto, así como las variaciones en el nivel de compresión del ensamble, las cuales afectan directamente la resistencia interfacial [@ref12;@ref58;@ref57].
En este contexto, el presente trabajo se orienta a evaluar el comportamiento de la resistencia eléctrica de una celda electroquímica a partir de curvas de polarización (I-V). Las variables eléctricas del sistema se adquieren mediante instrumentación de alta resolución, lo que permite registrar de manera confiable la respuesta del electrolizador bajo diferentes condiciones de excitación y analizar su comportamiento en el dominio del tiempo, sin requerir técnicas de caracterización más especializadas.
La evolución de la resistencia a lo largo de las distintas etapas de operación puede constituir un indicador del estado de la celda electroquímica. Además, el análisis de las curvas permite identificar regiones de operación en las que el sistema presenta mayores pérdidas de eficiencia, asociadas a una mayor disipación de energía en forma de calor. De este modo, la metodología propuesta ofrece una alternativa de análisis más simple y accesible, sin comprometer la confiabilidad del estudio, y establece una base para el desarrollo de futuros métodos de monitoreo, control y optimización energética en celdas electroquímicas.
@here
Metodología
Para poder llevar acabo las mediciones y obtener las curvas de polarización, se construyo un electrolizador de agua alcalino de laboratorio con electrodos de acero inoxidable (AISI 304) y electrolito acuoso de hidróxido de sodio (NaOH, 1M). Para la medición de las variables de voltaje y corriente, la celda se instrumento con una fuente de voltaje CD programable y dispositivos de alta resolución para la toma de muestras de manera simultanea. El control de dichos dispositivos se realizo por medio de protocolos de comunicación VISA (comandos SCPPI), de esta manera se automatiza la toma de muestras reduciendo asi el error por manipulación manual.
Con el objetivo de garantizar una reproducibilidad del experimento se hace uso de una plataforma gráfica basada en python para: (i) configurar los puntos de prueba del barrido, (ii) adquirir y almacenar las variables eléctricas de manera automática y sistemática, y (iii) generar las curvas de tensión–corriente del sistema. También se incorpora un sensor de temperatura PT1000 con el objetivo de monitorear la temperatura a la cual se encuentra el electrolito durante la operación del electrolizador.
La forma en como se llevo acabo la experimentación consistió en una sola prueba o experimento. A partir de los datos adquiridos, se calcularon los parametros eléctricos asociados a las curvas de polarización, asi como la resistencia eléctrica en cada punto de las curvas.
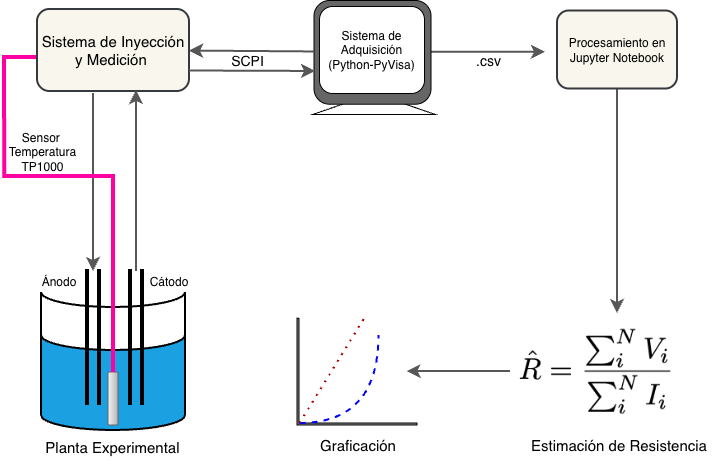
La @fig:Met_gral muestra el diagrama general de la metodología implementada en el presente trabajo.
Planta Experimental
Desde la perspectiva de identificación de sistemas, el electrolizador se modela como una planta experimental conformada por 3 partes: electrodos, electrolito y carcasa. Los electrodos constituyen la interfaz electroquímica encargada de inyectar la corriente en el medio acuoso (electrolito), estos al estar expuestos a las reacciones químicas derivadas de la ruptura de la molécula del agua (H_2 O), deben ser diseñados a partir de un material capaz de soportar la corrosión para mantener condiciones de operación estables.
El material seleccionado para la manufactura de los electrodos es Acero Inoxidable 304 y las dimensiones seleccionadas para el diseño de los electrodos son 20mm x 93mm, teniendo una area expuesta de 90mm^2. Los electrodos estarán inmersos en un electrolito de solución acuosa de 1 M de hidróxido de sodio (NaOH), este al ser un elemento altamente corrosivo se opta por el diseño de una carcasa integrada por un recipiente de vidrio y una tapa impresa en 3D fabricada en polipropileno.
La inyección de energía al electrolizador será por medio de una fuente de voltaje CD programable Agilent N5770A la cual cuenta con una capacidad máxima de potencia de 1500W. Para la medición de las variables de voltaje y corriente se hace uso de dos multímetros de precisión, el primero un Picotest M3500A reservado para la medición del voltaje y el segundo un Tektronix DM4040 parta la medición de corriente.
Todos los instrumentos empleados para la inyección de energía al sistema, así como la medición de las variables, cuentan con un protocolo de comunicación VISA (Virtual Instrument Software Architecture), la cual es una API (Interfaz de Programación de Aplicaciones) estandarizada para la comunicación con equipos de prueba mediante interfaces USB y RS-232. El control de estos dispositivos se llevo acabo a traves de una interfaz gráfica desarrollada en Python, la cual emplea la herramienta NI-VISA a traves del uso de la librería PyVISA para el envío de comandos SCPI (Standard Commands for Programmable Instruments), dichos comandos son las instrucciones necesarias para la configuración de dichos dispositivos y la extracción de las mediciones obtenidas así como la inyección precisa de energía en el sistema.
Los datos obtenidos son almacenados y desplegados en tablas donde se muestran las siguientes variables: No de Muestra, Voltaje Inyectado, Voltaje en los Electrodos, Corriente en los Electrodos, Corriente Inyectada, Resistencia Eléctrica, Temperatura y Observaciones. Estas variables finalizar la experimentación serán procesada y seleccionadas para el despliegue en gráficas donde se podrá observar el comportamiento del sistema a través de todo el experimento.
Protocolo de Experimentación
Para la caracterización del sistema se estableció una sola prueba o ronda de 4 experimentos. En cada experimento se busco replicar las mismas condiciones con el fin de buscar la repetibilidad del comportamiento de la celda electroquímica. No obstante, existen variables externas -principalmente la temperatura ambiente— que no pueden controlarse por completo, por lo que entre experimentos pueden presentarse variaciones térmicas ligeras.
En cada experimento se utiliza el mismo par de electrodos y el mismo electrolito, con el objetivo de observar si el desgaste de estos componentes influye en el comportamiento de las variables eléctricas. Cada experimento sigue el siguiente procedimiento:
- Se aplican incrementos de
0.1 Ven la inyección de voltaje a la planta experimental, avanzando de manera progresiva hasta alcanzar el límite de corriente que puede suministrar la fuente de alimentación, que es de10.5 A. - Se establece un tiempo de espera aproximado de 1 minuto entre cada incremento para permitir la estabilización de las mediciones.
- Para cada punto se obtiene un promedio de cinco muestras por parámetro medido y se registra en la tabla.
Resultados
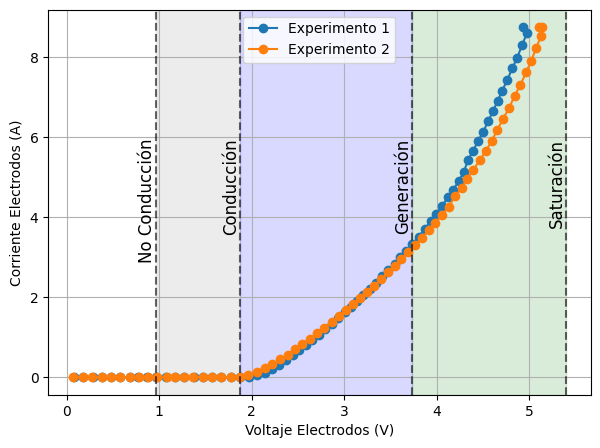
Una vez obtenidos los datos de los experimentos se procesan por medio de un algoritmo desarrollado en python y se organizan para realizar la comparación de la evolución de las variables a traves del desarrollo de los experimentos. La @fig:ve_ce muestra una gráfica comparativa de la evolución de la corriente en los electrodos a traves de 2 experimentos.
En la @fig:ve_ce se identifican claramente cuatro zonas de operación diferenciadas mediante colores, las cuales representan las distintas etapas por las que atraviesa el sistema electroquímico conforme aumenta el voltaje aplicado a la celda. Estas zonas permiten describir el comportamiento eléctrico del electrolizador y facilitan la interpretación del proceso de generación de hidrógeno.
La Zona 1, denominada No conducción, corresponde al régimen en el cual aún no existe un flujo significativo de electrones entre el ánodo y el cátodo. En esta etapa la resistencia electroquímica del sistema es elevada y el potencial aplicado no es suficiente para superar la barrera energética necesaria para iniciar el transporte de carga a través del medio electrolítico. En consecuencia, la corriente medida permanece cercana a cero. Este comportamiento se observa aproximadamente en el intervalo de 0.1 V a 1.0 V de voltaje aplicado.
Posteriormente se identifica la Zona 2, correspondiente al régimen de Conducción, donde el potencial aplicado comienza a superar la barrera de conducción del sistema. En esta región se inicia el flujo de electrones entre los electrodos y se observa un incremento gradual en la corriente medida. Las variables eléctricas presentan un comportamiento más estable conforme aumenta el voltaje aplicado; sin embargo, el potencial aún no es suficiente para activar de manera significativa la reacción electroquímica de descomposición del agua (H_2O). Este régimen se presenta aproximadamente en el intervalo de 1.1 V a 1.8 V.
La Zona 3, denominada Generación, corresponde al régimen donde se inicia el proceso de electrólisis del agua. En esta región se observa de manera visual la formación de gas en los electrodos, generándose hidrógeno en el cátodo y oxígeno en el ánodo. Desde el punto de vista eléctrico, el sistema presenta un comportamiento aproximadamente lineal entre el voltaje aplicado y la corriente medida, lo cual indica que el proceso electroquímico se encuentra operando en un régimen estable de generación. Este comportamiento se observa aproximadamente entre 1.9 V y 4.5 V.
Finalmente, la Zona 4, denominada Saturación, corresponde al régimen en el cual el sistema comienza a presentar un incremento significativo en la temperatura debido a la disipación de energía en forma de calor. En esta etapa el comportamiento del proceso se vuelve predominantemente exotérmico, lo cual indica que una fracción importante de la energía suministrada ya no se emplea únicamente en la reacción electroquímica, sino que se disipa térmicamente en el sistema. Si esta condición no se controla adecuadamente, puede conducir a la generación de vapor de agua, lo cual podría afectar la pureza del hidrógeno producido. Esta región inicia aproximadamente a partir de 4.5 V, extendiéndose hasta el límite máximo de voltaje permitido por la fuente de alimentación utilizada durante el experimento.
El calculo de la resistencia eléctrica se basa en los valores obtenidos de las variables de Voltaje en Electrodos (V) y Corriente en Electrodos (A), estos datos tienen un promediado de 5 muestras, las cuales son tomadas cada 100ms. La [@eq:calc_res] es la empleada para el estimación del valor de la resistencia en cada punto del experimento.
\mathrm{\hat{R} = \frac{\sum_{i}^{N}V_i}{\sum_{i}^{N}I_i}}
$$ {#eq:calc_res}
Partiendo de la división de las 4 distintas zonas, se analiza el comportamiento de la resistencia eléctrica dentro de la zona de saturación. La @fig:res_sat muestra el comportamiento de la resistencia del *Experimento 1* y *Experimento 2*.
{#fig:res_sat width=75%}
En esta zona de saturación se observa una diferencia clara entre los valores de resistencia. Aunque las curvas presentan una tendencia decreciente de la resistencia aun dentro del régimen de saturación, existe un desplazamiento notable entre ellas. Este “desfase” no debe interpretarse únicamente como una variación puntual del valor de resistencia, sino como una modificación en la respuesta eléctrica global del sistema para un mismo nivel de energía inyectada.
Al comparar la curva del *Experimento 1* con la del *Experimentos 2*, se aprecia que, para un mismo voltaje aplicado, la caída de tensión en los electrodos es mayor. Sin embargo, esto no implica necesariamente un mejor flujo de corriente. Por el contrario, indica que una fracción significativa de la energía suministrada se está concentrando en forma de potencial eléctrico en los electrodos, en lugar de transformarse eficientemente en corriente que favorezca la separación de la molécula de agua.
Este comportamiento sugiere que el desgaste progresivo de los electrodos y las modificaciones en el electrolito influyen directamente en la distribución de la energía dentro del sistema. En consecuencia, el desplazamiento observado entre curvas refleja un cambio en el régimen de conducción eléctrica, donde el aumento de la caída de tensión no se traduce proporcionalmente en un incremento del flujo de corriente, evidenciando una alteración en la eficiencia electroquímica del proceso.
Como se menciono anteriormente la zona de saturación comprende el comportamiento del sistema donde la mayoría de la energía inyectada se disipa en forma de calor, lo cual se ve reflejado en el aumento de la temperatura dentro del sistema. Las @fig:res_temp muestran el comportamiento de la resistencia y la temperatura del *Experimento 1 y 2* en la transición de la Zona de *Generación* hacia la Zona de *Saturación*.
{#fig:res_temp width=100%}
Como se observa en la @fig:res_temp (a), el *Experimento 1* presenta una disminución progresiva de la resistencia durante la transición de la zona de *Generación* hacia la zona de *Saturación*. Aunque la resistencia continúa decreciendo en este intervalo, los cambios son graduales y se acompañan de un incremento moderado de la temperatura. Esta relación sugiere que, dentro de este régimen, una fracción significativa de la energía eléctrica suministrada se está empleando efectivamente en el proceso electroquímico de separación del agua, y no se disipa predominantemente en forma de calor. En consecuencia, el sistema mantiene un comportamiento relativamente estable desde el punto de vista térmico y eléctrico.
En contraste, el *Experimento 2* exhibe un comportamiento distinto. Si bien la resistencia también muestra una tendencia decreciente en la zona de *Generación*, el aumento de la temperatura se manifiesta de manera más temprana y con una pendiente más pronunciada desde el inicio de dicha región. Este crecimiento térmico anticipado indica que una mayor proporción de la energía inyectada se está disipando como calor, lo cual sugiere un incremento en las pérdidas internas del sistema. En términos físicos, este comportamiento puede asociarse a un aumento de la contribución resistiva efectiva (ya sea por desgaste superficial de los electrodos, modificaciones en el electrolito o acumulación de burbujas en la interfaz) que altera la distribución energética y reduce la eficiencia electroquímica global del proceso.
# Conclusiones
---
Anotaciones: 0,21250 SHA-256 0a4b3852d7098fb3933e
@Guillermo <Memo>: 523,129 663,12 676,36 729,3 760 764,16 837,37 876 902,4 941,7 995 2653,31 2685 2687,3 2691 2713,2 2725,12 2738 2747,56 2874 2917 2921,11 2990,22 3013 3029,15 3053,9 3063,20 3086,22 3109 3130,49 3869
@Gerardo Marx <gmarx>: 346,177 652,11 675 712,17 732,28 761,3 780,57 874,2 877,25 906,35 948,47 996 1649,5 1784 2010,626 2637,16 2684 2686 2690 2692,21 2715,10 2737 2739,8 2803,71 2875,42 2918,3 2932,58 3012 3014,15 3044,9 3062 3083,3 3108 3110,20 3868 4411,12 4677,32 4980,26 5007,7
...